目前,治疗性抗体在治疗癌症、肿瘤、自身免疫性疾病、慢性炎症、感染性疾病等领域取得了重大进展,抗体工程的发展进一步推动新型抗体的产生。截至2022年年底已上市的治疗性抗体药物及其衍生物超过100种。基于实用性和功能上的考虑,现在临床上使用的治疗性抗体大多为IgG类型。
在开发治疗性抗体时,IgG亚型的选择是基于其体外活性可以推断体内活性的假设。亚型是决定治疗性抗体的体内生物学活性的关键因素之一。除亚型外,IgG-Fc糖型、抗原决定簇密度、细胞Fc受体多态性等多个参数也共同影响着治疗性抗体体内功能结果,导致准确预测治疗性抗体的体内活性仍有困难。因此在抗体药物设计中应把亚型的结构特征与目的效应功能的关联、体外IgG-Fc和效应配体之间相互作用的分子机制、亚基的生物学活性、理化性质等纳入综合考虑,以确保最大的疗效和安全性。
虽然IgG各亚型在体外实验评估中呈现特定的效应功能,然而在不同疾病中各亚型体内的作用方式可能有所不同。因此,在治疗性抗体的开发中为达到期望的治疗效果并且避免不良反应,选择适宜的抗体亚型就显得格外重要。
IgG可根据其在血清中的分布丰度进一步分为IgG1(60%)、IgG2(25%)、IgG3(10%)、IgG4(5%)4种亚型,它们的恒定区序列高度同源。4种IgG亚型其恒定区的CH2区不同、铰链区的核心CXXC序列组成不同,重链和轻链之间的二硫键连接方式也不同。
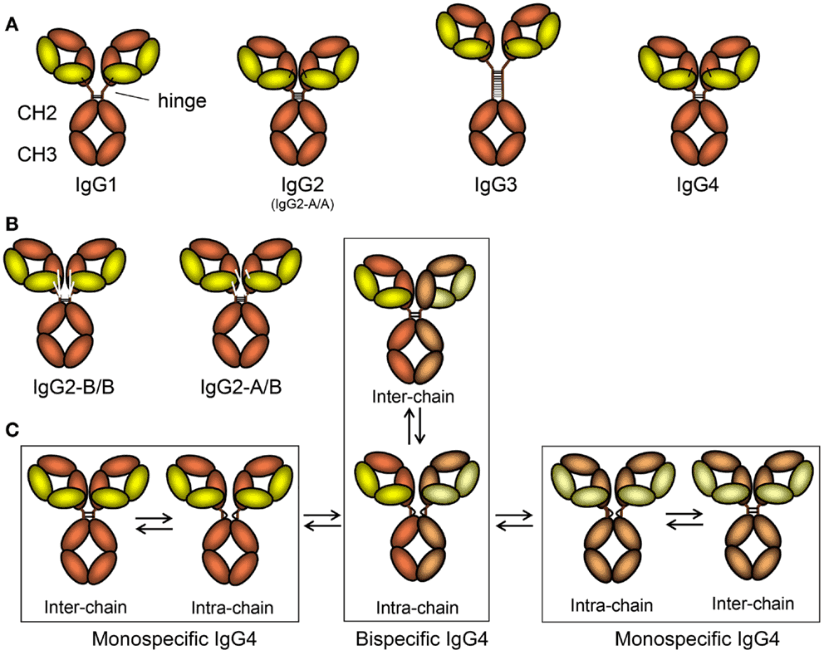
图1 IgG亚型及其异构体示意图
(A)不同的IgG亚型重链和轻链结构、铰链的长度以及连接两条重链的二硫键的数量。
(B)显示了IgG2的B/B形式(重链间只有两个二硫键,并存在重轻链间的替代连接)以及中间A/B形式。
(C)IgG4的异构体导致半分子交换。
表1 IgG各亚型的结构差异
| IgG1 | IgG2 | IgG3 | IgG4 | |
|---|---|---|---|---|
| 分子质量(kDa) | 146 | 146 | 170 | 146 |
| 活性形式 | 二价单体 | 四价二聚体 | 二价单体 | 单价半抗体 |
| 同型 | 4 | 1 | 13 | 0 |
| 铰链区氨基酸个数 | 15 | 12 | 62a | 12 |
| 铰链区链内二硫键的个数 | 2 | 4b | 11a | 2 |
a:Depends on allotype;b:A/A isomer.
人类Fcγ受体家族包括六个成员,它们在细胞分布、与Fc的结合亲和力以及产生的生物活性方面有所不同。功能上最相关的FcγR是FcγRI,FcγRIIA,FcγRIIB和FcγRIIIA。FcγRI是一种对IgG具有高亲和力的激活受体,可以被单体IgG激活。除了FcγRI外,所有其他FcγR只有在抗体与特定抗原结合时,其Fc区才能激活下游效应功能。FcγRIIB是唯一的抑制性FcγR,在许多免疫细胞上表达,包括B细胞,单核细胞,巨噬细胞,DC和肥大细胞。当IgG与抗原结合时,FcγRIIB通过胞内免疫受体酪氨酸抑制基序(ITIM)转导抑制信号,抑制ADCC和ADCP。最典型的激活FcγR是FcγRIIA和FcγRIIIA。FcγRIIA主要在单核细胞和巨噬细胞上表达,而FcγRIIIA主要在NK细胞上表达。两种激活的FcγR都有两种等位基因变体。
与结构相适应,4种IgG亚型与抗原结合、免疫复合物的形成、补体激活、触发效应细胞、半衰期和胎盘转运特性均具有特异性。表2总结了IgG亚型功能特征的差异。
在4个IgG亚型中,IgG3与大多种类的FcγR的亲和力结合度最高,但由于其长铰链区和多态性,这两者都增加了稳定性和免疫原性的风险,未能成为治疗性抗体的常规选择。在其余亚型中,IgG1对所有FcγR表现出最高的亲和力,并且可以有效激活ADCC和ADCP反应。IgG4仅对FcγRI具有高亲和力,对其他受体的亲和力较弱,其Fc介导的效应功能较弱。IgG2对FcγRIIAH131形式具有高亲和力,但对FcγRI和其他FcγR没有可测量的或微弱的亲和力。
表2 IgG各亚型的功能差异
| IgG1 | IgG2 | IgG3 | IgG4 | |||||
|---|---|---|---|---|---|---|---|---|
| 体内生物学活性 | 蛋白质抗原 | 糖类抗原 | 蛋白质抗原 | 响应慢性刺激、抗炎活性 | ||||
| 半衰期(天) | 21 | 21 | 7~21a | 21 | ||||
| 胎盘转运 | ++++ | ++ | ++/++++a | +++ | ||||
| 与下列物质的抗体反应 | ||||||||
| 蛋白质 | ++ | +/- | ++ | ++e | ||||
| 多糖 | + | +++ | +/- | +/- | ||||
| 过敏源 | + | (-) | (-) | ++ | ||||
| 补体激活 | ||||||||
| 结合C1q | ++ | + | +++ | – | ||||
| Fc受体 | ||||||||
| FcgRI | +++ | 65d | – | – | +++ | 61 | ++ | 34 |
| FcγRIIaH131 | +++ | 5.2 | ++ | 0.45 | ++++ | 0.89 | ++ | 0.17 |
| FcγRIIaR131 | +++ | 3.5 | + | 0.10 | ++++ | 0.91 | ++ | 0.21 |
| FcγRIIb/c | + | 0.12 | – | 0.02 | ++ | 0.17 | + | 0.20 |
| FcγRIIIaF158 | ++ | 1.2 | – | 0.03 | ++++ | 7.7 | – | 0.20 |
| FcγRIIIaV158 | +++ | 2.0 | + | 0.07 | ++++ | 9.8 | ++ | 0.25 |
| FcγRIIIb | +++ | 0.2 | – | – | ++++ | 1.1 | – | – |
| FcRn (at pH < 6.5) | +++ | +++ | ++/+++a | +++ | ||||
a:Depends on allotype;b:A/A isomer;c:Multivalent binding to transfected cells;
d:Association constant (×106 M-1) for monovalent binding; e:After repeated encounters with protein antigens, often allergens
多达12个在肿瘤细胞上表达的靶标已经过临床验证。除靶向EGFR的西妥昔单抗和帕尼单抗分别选择IgG1和IgG2亚型外,所有其他靶标均选择了IgG1亚型。Her2和EGFR属于酪氨酸激酶受体家族,靶向抗体可能通过阻断生长信号发挥抗肿瘤活性,除此之外IgG1抗体诱导的针对受体酪氨酸激酶(RTK)的ADCC和/或ADCP也起着重要的治疗作用。因此,在开发靶向肿瘤细胞上靶标的治疗性抗体时,主要考虑IgG1,它对激活FcγR具有最佳的结合亲和力,可以引起针对肿瘤细胞的强ADCC和/或ADCP活性。此外,当ADCP被激活时,效应细胞(巨噬细胞或树突状细胞)可能会将处理后的肿瘤抗原呈递给T细胞,从而进一步引发持久的肿瘤特异性适应性免疫。
一些肿瘤细胞靶标是免疫检查点(ICP)的配体,例如PD-L1和CD47,它们分别是PD-1和SIRPα的配体。PD-1及其配体PD-L1通过逃避肿瘤中和免疫监视在肿瘤进展和存活中起至关重要的作用。PD-L1在肿瘤细胞和抗原呈递细胞中表达,与T细胞PD-1的结合导致肿瘤中的T细胞功能障碍、衰竭、中和和IL-10产生。因此,阻断PD-1或PD-L1识别过程可以阻断抑制信号传导,从而重新激活效应T细胞杀死肿瘤细胞。简单地阻断PD-L1可以诱导显著的治疗效果,但以IgG1形式保留Fc效应器功能将进一步提高治疗效果。据报道,阿维鲁单抗是一种IgG1亚型抗PD-L1抑制剂,可触发NK细胞介导的细胞毒性和细胞因子产生以对抗三阴性乳腺癌细胞。
ADCC的诱导取决于肿瘤细胞上靶标表达的丰度,每个细胞的最低需求为105~106。与肿瘤组织相比,正常组织通常表达水平要低得多。丰度小于105的细胞诱发可能小,因此不会受到ADCC的损害。
靶向免疫细胞靶标的IgG亚型选择更为复杂。由于细胞表达免疫抑制受体的分布不同,如PD-1、TIM-3和LAG-3主要在CD8 T淋巴细胞(免疫效应细胞)中表达,而CTLA-4主要在Treg细胞(免疫抑制细胞)中表达,在开发针对免疫抑制受体(ICP)的治疗性抗体时,应仔细考虑IgG亚型的影响。目前批准的所有PD-1抗体都是IgG4亚型形式,可见IgG4是PD-1抗体的首选形式。这是因为IgG4仅对FcγRI具有高亲和力,但对所有其他FcγR的亲和力较弱,不具有可检测的Fc介导的效应功能,这意味着CD8 T淋巴细胞不会被相应消除。
针对Tregs或其他免疫抑制细胞表达的ICP可以选择IgG1亚型抗体,这些细胞可以通过ADCC/ADCP被抗体清除。靶向CTLA-4的伊匹木单抗就是一种主要通过ADCC/ADCP消除TME中的Tregs细胞来发挥治疗效果的IgG1亚型抗体。而靶向CTLA-4的IgG2亚型替西木单抗自2006年以来一直在进行广泛的临床试验。由于IgG2仅对FcγRIIaH131具有高亲和力,FcγRIIaH131主要在巨噬细胞中表达,在没有CD47-SIRPα阻断剂的情况下不会完全激活,因此替西木单抗将无法从TME中消除Tregs细胞。
免疫刺激受体大多数属于肿瘤坏死因子受体(TNFR)超家族(如4-1BB,CD40,OX40,CD27,GITR),经激动抗体结合后可刺激免疫。针对ICP受体的抗体单纯阻断靶点可激活T细胞,而通过抗体激活TNFR超家族成员需要抗体与FcγR交联。这表明FcγRIIB是靶向TNFR超家族成员免疫刺激受体的抗体所需要的。此外,CH1结构域中的铰链区也很重要,是抗体激动功能所必需的。给定IgG的铰链越硬,免疫刺激受体在细胞膜上的聚集越稳定,抗肿瘤功效越好。
总的来说,在开发靶向肿瘤抗原的抗体药物时,应优先考虑IgG1亚型,特别是当Fc介导的效应功能是肿瘤治疗的主要作用方式时。在选择免疫细胞中靶标的IgG亚型时,应仔细考虑靶标的性质。如果ICP在免疫效应细胞上表达,则应优先考虑IgG4。如果在Treg或其他免疫抑制细胞上表达,则应选择IgG1。对于具有免疫刺激功能的靶标,特别是TNFR超家族成员的靶标,除了表位筛选外,还应设计增强FcγRIIB参与。
参考文献
[1]Vidarsson G, Dekkers G, Rispens T. IgG subclasses and allotypes:from structure to effector functions. Front Immunol, 2014, 5 (520) : 1–17.
[2]吕若芸,陈忱,魏敬双. 治疗性抗体药物开发中IgG亚型选择[J]. 中国生物工程杂志, 2016, 36(7): 104-111.
[3]Yu J, Song Y, Tian W. How to select IgG subclasses in developing anti-tumor therapeutic antibodies. J Hematol Oncol, 2020, 13: 45.

亚美体育·(中国)在线登录 Nanjing Detai Bioengineering Co.,Ltd. ©2024 All Rights Reserved
苏ICP备2021019379号-1 | 网站地图 | 用户协议 | 隐私政策